Введение. Фторхинолоны (офлоксацин, ципрофлоксацин, моксифлоксацин) относятся к высокоэффективным лекарственным средствам и обладают широким спектром антимикробного действия. Нами разработаны новые 0,5% мази «Офлоксазоль», «Ципрофлоксазоль», «Моксифлоксазоль», изготовленные на титансодержащей основе [3, 5]. Гель «Тизоль» в исследуемых мазях является активатором проведения лекарственных веществ и обеспечивает дополнительные терапевтические эффекты: антифлогистический, антибактериальный, анальгетический [2, 6].
Согласно литературным данным, метод производной спектрофотометрии перспективно применять для качественного анализа лекарственных средств [7-10]. Предлагаемый метод основывается на вычислении производных оптической плотности различного порядка от длины волны и построении спектральных кривых производной с отчетливыми экстремумами. Идентификация лекарственных средств производится путем установления положения экстремальных точек и расчета производной молярного показателя поглощения [1, 4].
Цель исследования. Разработка методики качественного анализа лекарственных средств производных фторхинолона в мазях с применением второй производной спектрофотометрии.
Материалы и методы. Объектами исследования являются субстанции офлоксацина, ципрофлоксацина и моксифлоксацина, соответствующие требованиям нормативной документации и 0,5% мази «Офлоксазоль», «Ципрофлоксазоль», «Моксифлоксазоль», изготовленные на титансодержащей основе. Для получения катионной и анионной форм фторхинолонов использовали 0,1 моль/л растворы хлористоводородной кислоты и гидроксида натрия.
Оптическую плотность растворов лекарственных средств измеряли на регистрирующем приборе СФ-2000 через 4 нм. Дифференцирование спектров проводили с помощью программного обеспечения спектрофотометра.
Результаты. Предварительно нами были изучены особенности ультрафиолетового поглощения фторхинолонов в средах с различным значением рН. Качественный анализ лекарственных средств проводили на основании построения производных второго порядка с интервалом Δλ = 4 нм в 0,1 моль/л растворах хлористоводородной кислоты и гидроксида натрия.
Для катионных форм субстанций офлоксацина, ципрофлоксацина и моксифлоксацина (Рис. 1-3, А, кривые 1) на кривых второй производной имеются минимумы в области 270-310 нм. Спектры анионных форм лекарственных препаратов характеризуются минимумами при 260-300 нм (Рис. 1-3, В, кривые 1). Найденные экстремальные точки на кривых второй производной соответствуют максимумам поглощения исходных спектров фторхинолонов в аналогичных средах.
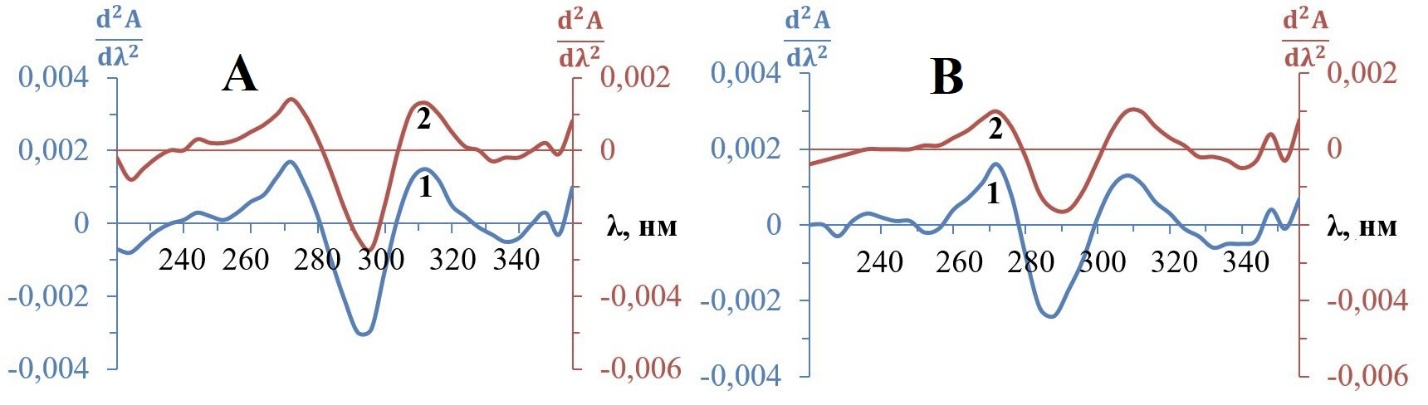
Рисунок 1. Спектральные кривые производных второго порядка катионной (А) и анионной (В) форм офлоксацина.
1 – офлоксацин (С = 2,0·10-5 моль/л); 2 – этанольная вытяжка офлоксацина из мази (С = 2,0·10-5 моль/л)
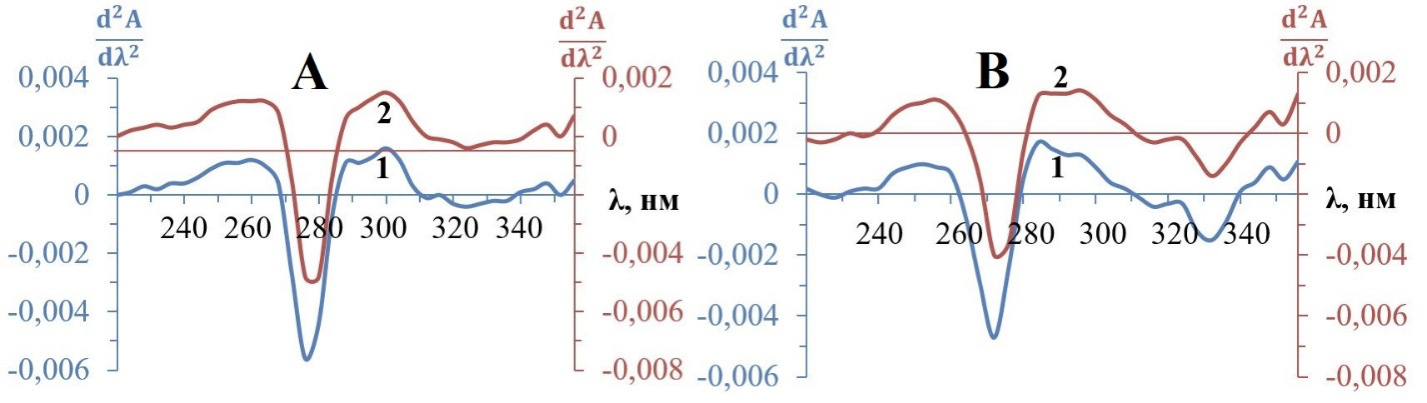
Рисунок 2. Спектральные кривые производных второго порядка катионной (А) и анионной (В) форм ципрофлоксацина.
1 – ципрофлоксацин (С = 2,0·10-5 моль/л); 2 – этанольная вытяжка ципрофлоксацина из мази (С = 2,0·10-5 моль/л)
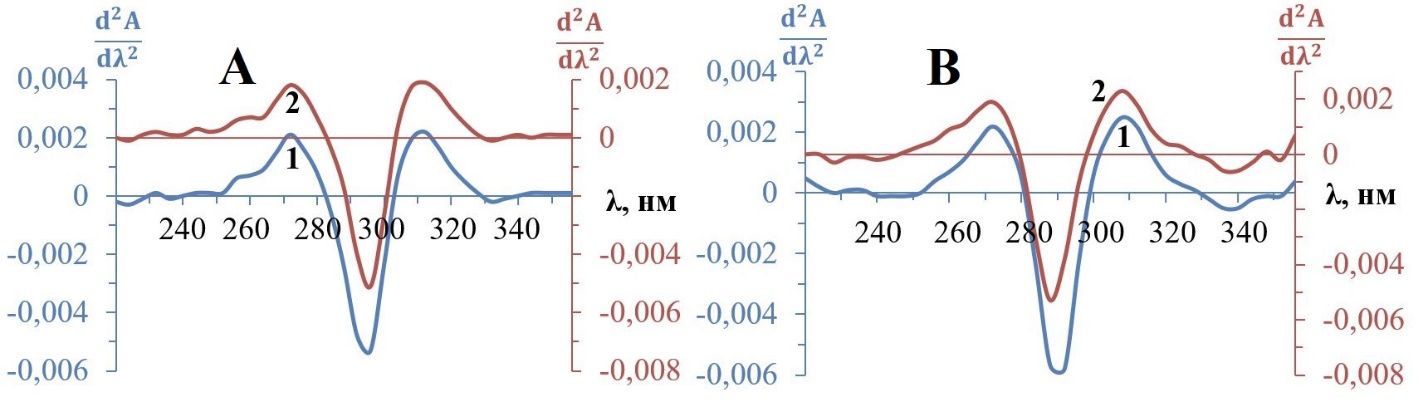
Рисунок 3. Спектральные кривые производных второго порядка катионной (А) и анионной (В) форм моксифлоксацина.
1 – моксифлоксацин (С = 2,0·10-5 моль/л); 2 – этанольная вытяжка моксифлоксацина из мази (С = 2,0·10-5 моль/л)
Спектры вторых производных, построенные нами для этанольных вытяжек из мазей фторхинолонов (Рис. 1-3, кривые 2), характеризуются неизменными экстремальными точками катионной и анионной форм лекарственных средств.
Следовательно, идентификацию фторхинолонов следует проводить на основании установления положения экстремумов на кривых второй производной и значений производной второго порядка молярных показателей поглощения. В таблице 1 приведены результаты расчета молярных коэффициентов в экстремальных точках на спектрах поглощения и кривых второй производной.
Таблица 1.
Значения молярных коэффициентов в экстремальных точках на спектрах поглощения и кривых второй производной
|
Лекарственная форма |
Среда |
Субстанция |
Мазь |
||
|
ε(λmax) |
ε''(λmax) |
ε(λmax) |
ε''(λmax) |
||
|
Офлоксазоль |
0,1 моль/л HCl |
ε(292) = 28400,00 |
ε''(292) = 2400,00 |
ε(292) = 25560,00 - 31240,00 |
ε''(292) = 2160,00 - 2640,00 |
|
0,1 моль/л NaOH |
ε(288) = 23820,00 |
ε''(288) = 1360,00 |
ε(288) = 21438,00 - 26202,00 |
ε''(288) = 1224,00 - 1496,00 |
|
|
Ципрофлоксазоль |
0,1 моль/л HCl |
ε(276) = 35935,00 |
ε''(276) = 4240,00 |
ε(276) = 32341,50 - 39528,50 |
ε''(276) = 3816,00 - 4664,00 |
|
0,1 моль/л NaOH |
ε(270) = 29190,00 |
ε''(270) = 3760,00 |
ε(270) = 26271,00 - 32109,00 |
ε''(270) = 3384,00 - 4136,00 |
|
|
Моксифлоксазоль |
0,1 моль/л HCl |
ε(292) = 36925,00 |
ε''(292) = 3840,00 |
ε(292) = 33971,00 - 39879,00 |
ε''(292) = 3532,80 - 4147,20 |
|
0,1 моль/л NaOH |
ε(288) = 36750,00 |
ε''(288) = 4560,00 |
ε(288) = 33810,00 - 39690,00 |
ε''(288) = 4195,20 - 4651,20 |
|
Примечание: ε(λmax) – молярный коэффициент в экстремальных точках спектров поглощения; ε''(λmax) – молярный коэффициент в экстремальных точках кривых второй производной.
Проведенные исследования позволили предложить способ качественного анализа фторхинолонов в мазях. Методика: к точной массе исследуемой мази (около 0,1 г) прибавляют 4-5 мл 0,1 моль/л раствора хлористоводородной кислоты и этиловый спирт до 30 мл (V(общ)). Полученную смесь фильтруют. Затем к 4,3-5,0 мл фильтрата (V1) прибавляют 0,1 моль/л раствор хлористоводородной кислоты (гидроксида натрия) до общего объема 10 мл (V2). Раствором сравнения служит этанольная вытяжка из геля «Тизоль», полученная аналогичным способом. Далее измеряют оптические плотности с помощью прибора СФ-2000 и дифференцируют спектры поглощения в программном обеспечении спектрофотометра. В таблице 2 представлены данные для вычисления производной второго порядка молярного коэффициента поглощения лекарственных средств в мазях.
Таблица 2.
Данные для расчета молярных коэффициентов поглощения второй производной лекарственных средств в мазях
|
№ п/п |
Лекарственное средство |
М, г/моль |
V1, мл |
V2, мл |
V(общ), мл |
V(HCl), мл |
|
1 |
Офлоксацин |
361,38 |
4,3 |
10,0 |
30,0 |
4,0 |
|
2 |
Ципрофлоксацин |
385,82 |
4,6 |
10,0 |
30,0 |
5,0 |
|
3 |
Моксифлоксацин |
437,90 |
5,0 |
10,0 |
30,0 |
5,0 |
Молярные коэффициенты поглощения второй производной в экстремальных точках рассчитывают по формуле (1).
|
|
(1) |
Где: 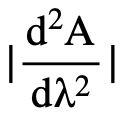 – модуль значения второй производной; dλ2 – квадрат интервала измерений; V(общ) – объем этилового спирта, растворяющий навеску мази, мл; m(ЛС) – масса лекарственного средства в прописи, г; М(ЛС) – молярная масса лекарственного средства, г/моль; a(мази) – навеска мази, взятая на анализ, г; V1, V2 – кратность разбавления; Р – общий вес лекарственной формы, г.
– модуль значения второй производной; dλ2 – квадрат интервала измерений; V(общ) – объем этилового спирта, растворяющий навеску мази, мл; m(ЛС) – масса лекарственного средства в прописи, г; М(ЛС) – молярная масса лекарственного средства, г/моль; a(мази) – навеска мази, взятая на анализ, г; V1, V2 – кратность разбавления; Р – общий вес лекарственной формы, г.
Заключение. На основании проведенных исследований изучены особенности кривых производной второго порядка фторхинолонов в 0,1 моль/л растворах хлористоводородной кислоты и гидроксида натрия. Разработана методика качественного анализа действующих веществ в мазях «Офлоксазоль», «Ципрофлоксазоль» и «Моксифлоксазоль» с применением второй производной спектрофотометрии. Предлагаемый способ анализа лекарственных средств может быть рекомендован для включения в нормативную документацию по исследованию мягких лекарственных форм.
Список литературы
- Вергейчик Е.Н. Разработка методов производной и дифференциальной спектрофотометрии для анализа лекарственных средств: автореферат дис. ... доктора фармацевтических наук: 15.00.02 / 1-й Моск. мед. ин-т им. И.М. Сеченова. – Москва. – 1988. – С. 33.
- Емельянов А.А., Махотина М.В., Петров А.Ю., Смагина Т.А. Аквакомплекс глицеросольвата титана (Тизоль®) - оригинальная основа (вспомогательное вещество) для получения лекарственных средств // Результаты современных научных исследований и разработок: сборник статей XIII Всероссийской научно-практической конференции, Пенза, 27 мая 2021 года. Пенза: Общество с ограниченной ответственностью «Наука и Просвещение». – 2021. – С. 220-225.
- Замараева А.И., Кобелева Т.А., Шаповалова Е.М., Попова М.И. Качественный спектрофотометрический анализ моксифлоксацина и стабильность лекарственной мази «Моксифлоксазоль» // Сб. матер. XVIII Международной научно-практической конференции «Современные научные исследования: Актуальные вопросы, достижения и инновации». Пенза, 20 апреля 2021 года. – Пенза: Наука и Просвещение, 2021. – С. 271-275.
- Карташов В.А., Чернова Л.В. Применение метода производной уф-спектрофотометрии для анализа кветиапина, выделенного из мочи // Новые технологии. – 2012. – № 2. – С. 236-240.
- Кобелева Т.А., Сичко А.И., Замараева А.И., Бессонова Н.С. Разработка способа анализа офлоксацина в комплексном препарате «Офлоксазоль» // Разработка и регистрация лекарственных средств. – 2021. – Т. 10, № 3. – С. 70-75.
- Кобелева Т.А., Замараева А.И., Сичко А.И., Бессонова Н.С. Глава 15. Актуальность применения геля «Тизоль» в изготовлении мазей и спектрофотометрии в исследовании лекарственных форм, приготовленных на титансодержащей основе // Монография «Инновационное развитие: потенциал науки, бизнеса, образования». Пенза: МЦНС «Наука и Просвещение», 2021. – С. 186-240.
- Федерякина А.С., Родионова Р.А. Применение производной спектрофотометрии для количественного определения действующих веществ лекарственного средства «Параскофен» // Вестник фармации. – 2009. – № 2(44). – С. 31-42.
- Шорманов В.К., Щербаков Д.П. Применение производных спектров второго порядка для оценки содержания мебендазола в таблетках // Курский научно-практический вестник Человек и его здоровье. – 2017. – № 4. – С. 120-124.
- Lopes FCC, Fonseca L, Moita GC and Ribeiro MVM: Development and validation of methods using derivative spectrophotometry for determination of dipyrone in pharmaceutical formulations. Int J Pharm Sci Res 2018; 9(6): 2201-10.
- Redasani, Vivekkumar & Patel, Priyanka & Marathe, Divya & Chaudhari, Suraj & Shirkhedkar, Atul & Surana, Sanjay. (2018). A review on derivative uv-spectrophotometry analysis of drugs in pharmaceutical formulations and biological samples review. Journal of the Chilean Chemical Society. 63. 4126-4134.



