Восстановление тканей или заживление происходит в любом живом организме после его повреждения. Восстановление после травмы может происходить двумя путями: регенерацией клеток или тканей с воссозданием нормальной структуры или путем заживления, приводящем к образованию рубца. В случае регенерации поврежденная или утраченная ткань замещается разрастанием окружающих неповрежденных клеток и тканей. Нормальная структура ткани восстанавливается или происходит полная регенерация эпидермиса, эпителия желудочно-кишечного тракта и кроветворной системы, где клетки обладают высокой пролиферативной способностью. В случае стабильных тканей, таких как печень и почки, происходит компенсаторный рост, а не истинная регенерация. Особенности процесса восстановления будут зависеть от способности ткани к регенерации и степени повреждения. Раны на поверхностной коже заживают за счет регенерации поверхностного эпителия, однако восстановление исходного внеклеточного матрикса, поврежденного тяжелой травмой, включает отложение коллагена и образование рубцов (репарация посредством рубцевания), в результате чего нормальная структура ткани необратимо изменяется [1]. Актуальные исследования в сфере регенеративной медицина сосредоточены на исследовании протеома (молекулярных механизмов, миграции и пролиферации клеток, молекул‑регуляторов и молекулярных мишеней для стимуляции эндогенного регенераторного потенциала организма) [2]. Исследования генов, участвующих в регенерации тканей, необходимо для лучшего понимания механизмов репарации и разработки новых методов лечения, направленных на стимуляцию регенерации тканей и восстановление их функции [3].
Цель настоящей работы – анализ актуальных сведений о генах, участвующих в процессе регенерации тканей человека.
Материалы и методы.
Выполнен поиск русско- и англоязычных литературных источников по теме статьи. После предварительного поиска статей за последние 5 лет в поисковых системах Яндекс и Google проведен более глубокий мониторинг статей в специализированных базах Cyberleninka, eLibrary, PubMed, ScienceDirect. Всего найдено 15 статей, информация в которых была проанализирована, обобщена. С помощью методов анализа, синтеза и дедукции были определены достижение генетических исследований в области регенерации тканей человека.
Результаты и их обсуждение.
Генетические механизмы процесса регенерации изучаются в норме и рассматриваются возможности их модификации с целью расширения и повышения возможностей регенеративной медицины.
Генетика процесса регенерации. Известно, что гены регенерации тканей организма ответственны за активацию клеток, участвующих в процессе репарации, их дифференцировку и передаче сигналов между ними. Именно гены активируют участие стволовых клеток в регенерации тканей и контролируют в целом процесс репарации посредством активации белков, в частности факторов роста, стимулирующих деление и миграцию клеток, или протеиновой матрицы, необходимой для регенерации тканей. Описано участие генов в процессах воспаления посредством регуляции продукции воспалительных медиаторов и цитокинов, участвующих в активации иммунных клеток [3].
Исследования в области регенерации проводятся для изучения особенностей восстановления конкретных типов тканей. Крайне актуальной является изучение особенностей регенерации костной ткани [4], так как необходимо преодоление нарушений репаративных проблем при заживлении костей после переломов в современной травматологии и ортопедии [5]. Клинические наблюдения показали, что существуют пациенты без системных или местных факторов риска и предрасположенностью к нарушениям консолидации переломов. Определен ряд механизмов влияния иммуногенетики человека на развитие нарушений консолидации костей [6, 7]. Генетические факторы приводят к аномальной экспрессии цитокинов (рис. 1), от которой зависит консолидация костной ткани [6].
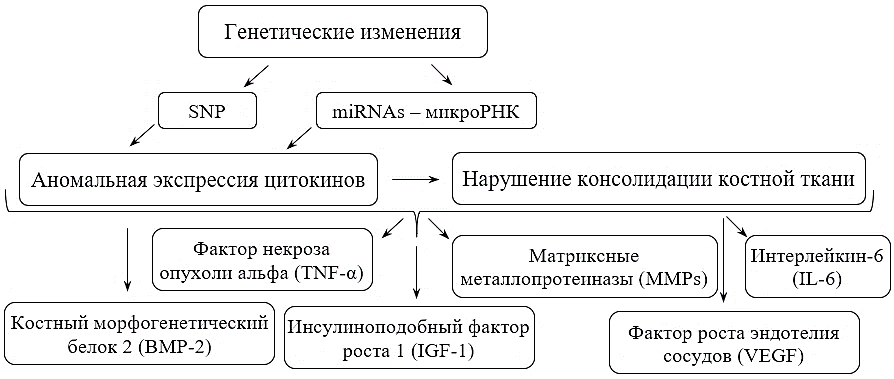
Рисунок 1. Патогенез нарушения консолидации костной ткани на молекулярно-генетическом уровне. Составлено по данным [6].
Проведены сравнительные исследования локальной экспрессии генов в месте перелома у пациентов с нормальной консолидацией повреждения и ее нарушением. Обнаружены генетические аллели, влияющие на процесс регенерации костной ткани (табл. 1) и выделены защитные факторы: генотипы G/G генов матриксной метеллопротеиназы – MMP13 (rs3819089) и костного морфогенетического белка 6 – BMP6 (rs270393), а также генотипы G/T и G/G растворимого фактора дифференцировки остеобластов – FAM5C (rs1342913) были ассоциированы с нормальным заживлением перелома кости. Установлено также, что экспрессия генов в зоне нарушенной консолидации выше, чем в условиях нормального формирования молодой костной мозоли, что может нарушать структуру и функцию клеток в области перелома. К таковым относятся гены белков CDO1, COMP, FMOD, FN1 (участников формирования и стабилизации внеклеточного матрикса), CLU и TCS22 (индукторы клеточной дифференцировки и пролиферации), ACTA2 и PDE4DIP (участники формирования и поддержания цитоскелета). Выявлено также, что микроРНК являются регуляторами экспрессии генов, в том числе формирование, резорбцию и ремоделирование костей, способствуя заживлению переломов или несращению [4].
Таблица 1.
Примеры генетических аллелей, увеличивающих риск нарушения консолидации костной ткани после переломов
|
Аллель |
Эффект |
|
Гомозигота SNP гена TGFβ1 (Arg25Pro) |
Экспрессия TGFβ1 – трансформирующего фактора роста бета-1 снижается |
|
Гомозигота SNP гена EGFR (A2073T) |
Экспрессия EGFR – рецептора эпидермального фактора роста снижается |
|
Hox-гены – регуляторы МСККС: гомозиготы SNP генов (1) NOGGIN (G/G rs1372857) и (2) SMAD6 (T/T rs2053423) |
Снижение экспрессии белков: (1) участвует в развитии тканей, включая нервную ткань, мышцы и кости; (2) действует как регулятор активности семейства TGFβ и регуляции органогенеза у эмбриона. |
|
Гаплотип А тромбоцитарного фактора роста (PDGF) (rs1800814, rs62433334, rs13309625; CCG) |
Ассоциирован с не сращиваемыми диафизами бедренной и большеберцовой костей. |
|
Аллели T и C/T кодона 10 гена TGF‑β и мутантного гена TLR4 W/1 (толл-подобный рецептор) |
Возможно, факторы риска снижения эффективности распознавания и элиминирования бактерий, повышают вероятность развития септического нарушения консолидации. |
|
Генотипы C/T или T/T гена IL1β (rs2853550); генотип T/G CYR61 (богатый цистеином ангиогенный индуктор 61) (rs3753793) |
Функции сигнальной молекулы во многих путях, возможно, способствование формирования не сращиваемого повреждения. |
Примечание: составлено по данным [4, 6], SNP – однонуклеотидный полиморфизм, МСККС – мезенхимальные стволовые клетки костного мозга.
Выполнены исследования регенерации генов скелетных мышц, участвующих в ремоделировании внеклеточного матрикса и сосудистой сети, а также в мышечных реакциях на силовые тренировки. Известно, что после иммобилизации поврежденной мышцы, часть пациентов отвечает положительно на реабилитацию (физические упражнения, механотерапию, механотрансдукцию) ранее обездвиженной мышцы, реакции других слабы. Выявлено, что экспрессия у пациентов с хорошим и плохим ответом на реабилитацию включает 3313 и 1710, 4124 и 3138, 2627 и 1693 генов до, во время и после реабилитации в зоне повреждения соответственно. Так, у двух групп пациентов экспрессируются различные гены убиквитин-протеасомального протеолиза (системы расщепления мышечных долгоживущих белков) с более низкой экспрессией у пациентов с хорошим ответом на лечение и реабилитацию. Выявлены гены, активирующиеся специфически только у пациентов с хорошим ответом: ILK‑сигналинга (интегрин-связанной киназы), связанной с множеством клеточных функций, включая миграцию клеток, пролиферацию и адгезию; путей антигенной презентации и Fcγ-рецептора опосредованного фагоцитоза в макрофагах и моноцитах. В группе с плохим ответом отмечена активация пути передачи сигналов от актинового цитоскелета [8]. Выявлено также, что Трансформирующий фактор роста β1 индуцирует экспрессию коллагена I типа и механочувствительных генов маркерных белков, необходимых для теногенеза (регенерации сухожилия) [9].
Многие органы регенерируются за счет пролиферации клеток, заменяющих те, которые погибли в результате старения или повреждения. Однако пролиферация в значительной степени отсутствует в определенных критических органах, включая сердце, центральную нервную систему и органы чувств (внутреннее ухо и сетчатка). Биохимический сигнальный путь Hippo-Yap – каскад белков, ингибирующий деление клеток, представляет собой одно из препятствий для пролиферации. Сигнальный путь Hippo действует как тормоз регенерации во многих тканях. Этот каскад киназ завершается фосфорилированием кофакторов транскрипции Yap и Taz, концентрация которых в ядре остается низкой. Однако различные типы клеточных сигналов могут снижать фосфорилирование, что приводит к накоплению Yap и Taz в ядре и впоследствии к митозу [10].
Печень обладает замечательной способностью к быстрой регенерации после острого зонального повреждения. Для изучения этого процесса необходимо учитывать пространственную гетерогенность типов клеток печени [11]. Фазы регенерации печени включают: инициацию (сверхэкспрессию определенных генов для подготовки клеток печени к репликации); пролиферацию (серию циклов клеточного деления и размножения); остановки процесса регенерации [12]. Макрофаги являются критическими компонентами врожденной иммунной системы, и их активация необходима для инициации регенерации печени [13]. Интерлейкин-6 (IL‐6) и фактор некроза опухоли (TNF‐α), происходящие из макрофагов, ответственны за активацию ~ 40% непосредственных ранних генов, и истощение макрофагов может значительно снизить скорость регенерации печени. TNF‐α играет важную роль на этапе инициации, а IL-6 также рассматривается как критический компонент в подготовке гепатоцитов к пролиферации. Последний связывается со своим рецептором (комплексом субъединиц gp 80 и gp 130) на гепатоцитах. Активация субъединицы gp130 приводит к активности тирозинкиназы, которая фосфорилирует преобразователь сигнала и активатор транскрипции (STAT 3), а также внеклеточные протеинкиназы 1 и 2, регулируемые сигналом (ERK1/2), вызывая экспрессию множества генов-мишеней, важных для пролиферации гепатоцитов, таких как циклин D1 [12].
Аксонопатия является распространенным ранним признаком нейродегенеративных заболеваний центральной нервной системы (ЦНС), включая глаукому, которая характеризуется дегенерацией зрительного нерва с последующей прогрессирующей гибелью ганглиозных клеток сетчатки (ГКС) [14]. Аксоны ГКС у взрослых не регенерируют спонтанно после дегенерации, поэтому необходимы методы лечения восстановления нервной системы [15]. Делеция Pten (гомолог фосфатазы и тензина) в ГКС на сегодняшний день остается наиболее эффективной стратегией манипулирования одним геном для стимулирования регенерации зрительного нерва после его повреждения [16, 17].
Перспективы. Рассматривается потенциал восстановления утраченной части тела. В результате генетических исследований обнаружен ген р21, блокирующий регенерацию. Данный ген тесно связан с геном р53, ответственным за деление клеток и препятствующий образованию опухолей. Кроме того, он отвечает за блокировку деления клеток при поврежденной ДНК, т. е. развитию раковых опухолей [18, 19]. Известно, что ткань суставного хряща, обладающая низким потенциалом заживления, при травматическом повреждении подвергается дегенерации хряща и остеоартриту. Дефицит белка p21 способствовал заживлению повреждений суставного хряща у мышей, что было связано с пролиферацией клеток in vivo, но увеличение дифференцировки хондроцитов in vitro не наблюдалось [18]. На примере смоделированного метаболического повреждения печени на мышиной модели обнаружено, что контроль клеточного цикла при хроническом повреждении печени критически зависит от присутствия как p53, так и его последующего эффектора p21. В гепатоцитах с дефицитом p53 происходит неконтролируемая пролиферация, несмотря на сильную индукцию p21. Повышенный регенеративный потенциал в отсутствие p53 не может полностью компенсировать избыточное повреждение и недостаточен для содействия выживанию [19].
Идентифицирована небольшая молекула TRULI, которая блокирует конечные киназы в путях Lats1 и Lats2, что вызывает пролиферацию нескольких типов клеток, обычно являющихся постмитотическими, и способствует регенерации у млекопитающих. Химическая модификация TRULI позволила получить производное, TDI‑011536, которое является эффективным блокатором Lats-киназ in vitro в наномолярных концентрациях. Соединение способствует обширной пролиферации органоидов сетчатки, полученных из индуцированных плюрипотентных стволовых клеток человека. Внутрибрюшинное введение вещества мышам подавляет фосфорилирование Yap в течение нескольких часов и индуцирует активацию транскрипции генов-мишеней Yap в сердце, печени и коже. Более того, соединение инициирует пролиферацию кардиомиоцитов у взрослых мышей после криовоздействий на сердце [10].
Среди исследований применения стволовых клеток одним из наиболее значимых стало перепрограммирование соматических клеток человека в плюрипотентные эмбриональные стволовые клетки. Перспективы применения при успешных доклинических и клинических исследованиях включают: прорыв в лечении инфаркта миокарда, болезни Паркинсона, рассеянного склероза и повреждений позвоночника. В США и Японии получены клеточные вакцины из генно-модифицированных стволовых клеток с перспективой создания комбинированных препаратов с «терапевтическими» генами и компонентами доставки генетической информации [20]. Секретом мезенхимальных клеток стимулируют ангиогенез, рост нервов, а также подавляет воспаление [21], в частности благодаря присутствию нейротрофного фактора (тромбоцитарного фактора роста BDNF) и урокиназы (uPA) [22]. Плазмиды, несущие гены BDNF или урокиназы после ее внедрения в поврежденную зону позволяет прорастить сосуды или нервные окончания [21]. Совместное применение сразу двух генов оказалось эффективнее [23].
Регенерация аксонов имеет большие перспективы для восстановления нервной системы при аксонопатиях ЦНС, включая глаукому. Делеция Pten в ГКС способствует мощной регенерации зрительного нерва, так как только небольшая популяция ГКС, не содержащих Pten являются регенерирующей. Разработана стратегия специфического мечения и очистки регенерирующих ГКС у мышей с делецией Pten после повреждения зрительного нерва. Транскриптомный анализ отдельных клеток Smart-Seq2 выявил новые гены, которые значительно способствуют регенерации аксонов. Самый мощный из них, Anxa2, действующий синергично со своим лигандом tPA при регенерации аксонов, вызванной делецией Pten. Белок Anxa2 сохраняют зрительную функцию в клинически значимой модели глаукомы, демонстрируя захватывающий потенциал данной инновационной стратегии для выявления новых эффективных кандидатов на репарацию нервной системы [24].
Заключение
Многие проведенные исследования генетических аспектов регенерации требуют получения дополнительных данных с бóльшим количеством пациентов с соблюдением строгих критериев исключения в отношении сопутствующей патологии. Исследования генетических аспектов регенерации тканей включают изучение нормальных механизмов заживления и изучение нуклеотидных последовательностей, приводящих к аномалиям регенерации. Детально изучаются ткани, наиболее подверженные переломам и повреждениям, а именно, структуры опорно-двигательного аппарата, особенно кости. Обнаружено, что гены матриксной метеллопротеиназы и костного морфогенетического белка 6 (генотипы G/G) и растворимого факторы дифференцировки остеобластов (генотипы G/T и G/G) ассоциированы с нормальным заживлением перелома кости. Среди исследований генетических причин нарушения регенерации исследуются однонуклеатидные мутации генов. Перспективы развития регенеративной медицины на основе изучения генетических аспектов заживления тканей заключаются в применении генетической модификации поврежденного участка посредством выключения гена или внедрения генов, способствующих репарации поврежденной ткани.
После дальнейшей химической доработки родственные соединения могут оказаться полезными в защитной и регенеративной терапии.
Список литературы
- Paul W., Sharma C.P. Chapter 1 - Tissue and organ regeneration: An introduction / In book: Regenerated Organs, Academic Press, 2021. 3-9. https://doi.org/10.1016/B978-0-12-821085-7.00001-4
- Пронина Е.А., Попыхова Э.Б., Степанова Т.В., Иванов А.Н. Современные направления и перспективы развития регенеративной медицины // Современные проблемы науки и образования. – 2019. – № 3. URL: https://science-education.ru/ru/article/view?id=28968 (дата обращения: 15.01.2024)
- Биоинформатика и регенерация тканей: понятное объяснение и ключевые механизмы // Научные Статьи.Ру — портал для студентов и аспирантов. — Дата последнего обновления статьи: 28.11.2023. — URL https://nauchniestati.ru/spravka/identifikacziya-genov-svyazannyh-s-regeneracziej-tkanej/ (дата обращения: 14.01.2024)
- Мироманов А.М., Гусев К.А., Старосельников А.Н., Миронова О.Б., Мироманова Н.А. Современные генетические и иммунологические аспекты патогенеза нарушения консолидации переломов (обзор литературы). Acta biomedica scientifica. 2022; 7(2): 49-64. doi: 10.29413/ABS.2022-7.2.6
- Емельянов В.Ю., Преображенская Е.В., Николаев Н.С. Сравнительная оценка эффективности биофизических методов стимуляции остеогенеза: обзор литературы. Травматология и ортопедия России. 2021; 27(1): 86-96. doi: 10.21823/2311 -29052021-27-1-86-96
- Ding Z-C, Lin Y-K, Gan Y-K, Tang T-T. Molecular pathogenesis of fracture nonunion. J Orthop Translat. 2018; 14: 45-56. doi: 10.1016/j.jot.2018.05.002
- Zhang J, Yang Y, Yang Z, Li T, Chen F. Snapshot: Targeting macrophages as a candidate for tissue regeneration. Curr Issues MolBiol. 2018; 29: 37-48. doi: 10.21775/cimb.029.037
- Щербак С.Г., Макаренко С.В., Камилова Т.А., Голота А.С., Сарана А.М. Регенеративная реабилитация повреждений скелетных мышц. Клиническая практика. 2021;12(4): 51–65. doi: https://doi.org/10.17816/clinpract70873
- Kastan NR, Oak S, Liang R, Baxt L, Myers RW, Ginn J, Liverton N, Huggins DJ, Pichardo J, Paul M, Carroll TS, Nagiel A, Gnedeva K, Hudspeth AJ. Development of an improved inhibitor of Lats kinases to promote regeneration of mammalian organs. Proc Natl Acad Sci U S A. 2022;119(28):e2206113119. doi: 10.1073/pnas.2206113119
- Щербак С.Г., Макаренко С.В., Шнейдер О.В., Камилова Т.А., Голота А.С. Регенеративная реабилитация при повреждениях сухожилий. Физическая и реабилитационная медицина, медицинская реабилитация. 2021;3(2): 192–206. DOI: https://doi.org/10.36425/rehab70760
- Ben-Moshe S, Veg T, Manco R, Dan S, Papinutti D, Lifshitz A, Kolodziejczyk AA, Bahar Halpern K, Elinav E, Itzkovitz S. The spatiotemporal program of zonal liver regeneration following acute injury. Cell Stem Cell. 2022;29(6):973-989.e10. doi: 10.1016/j.stem.2022.04.008
- Abu Rmilah A, Zhou W, Nelson E, Lin L, Amiot B, Nyberg SL. Understanding the marvels behind liver regeneration. Wiley Interdiscip Rev Dev Biol. 2019;8:e340
- Michalopoulos GK, Bhushan B. Liver regeneration: biological and pathological mechanisms and implications. Nat Rev Gastroenterol Hepatol. 2021;18:40–55
- Calkins DJ (2021). Adaptive responses to neurodegenerative stress in glaucoma. Prog Retin Eye Res, 100953. 10.1016/j.preteyeres.2021.100953
- Wormald R, Virgili G, and Azuara-Blanco A (2020). Systematic reviews and randomised controlled trials on open angle glaucoma. Eye (Lond) 34, 161–167. 10.1038/s41433-019-0687-5
- Williams PR, Benowitz LI, Goldberg JL, and He Z (2020). Axon Regeneration in the Mammalian Optic Nerve. Annual review of vision science 6, 195–213. 10.1146/annurev-vision-022720-094953
- Zhang J, Yang D, Huang H, Sun Y, and Hu Y (2018). Coordination of Necessary and Permissive Signals by PTEN Inhibition for CNS Axon Regeneration. Front Neurosci 12, 558. 10.3389/fnins.2018.00558
- Ibaraki K, Hayashi S, Kanzaki N, Hashimoto S, Kihara S, Haneda M, Takeuchi K, Niikura T, Kuroda R. Deletion of p21 expression accelerates cartilage tissue repair via chondrocyte proliferation. Mol Med Rep. 2020 May;21(5):2236-2242. doi: 10.3892/mmr.2020.11028. Epub 2020 Mar 13. PMID: 32186772
- Buitrago-Molina LE, Marhenke S, Becker D, Geffers R, Itzel T, Teufel A, Jaeschke H, Lechel A, Unger K, Markovic J, Sharma AD, Marquardt JU, Saborowski M, Saborowski A, Vogel A. p53-Independent Induction of p21 Fails to Control Regeneration and Hepatocarcinogenesis in a Murine Liver Injury Model. Cell Mol Gastroenterol Hepatol. 2021;11(5):1387-1404. doi: 10.1016/j.jcmgh.2021.01.006. Epub 2021 Jan 21. PMID: 33484913; PMCID: PMC8024980
- Пронина Е.А., Попыхова Э.Б., Степанова Т.В., Иванов А.Н. Современные направления и перспективы развития регенеративной медицины // Современные проблемы науки и образования. – 2019. – №3.; URL: https://science-education.ru/ru/article/view?id=28968 (дата обращения: 15.01.2024)
- Ткачук В.А. Регенеративная биомедицина в биологии и медицине. Регенерация органов и тканей. 2023;1(1):7–15
- Sagaradze G., Grigorieva O., Nimiritsky P., et al. Conditioned medium from human mesenchymal stromal cells: Towards the clinical translation. International Journal of Molecular Sciences. 2019;20(7):e1656
- Karagyaur M., Rostovtseva A., Semina E., et al. A Bicistronic Plasmid Encoding Brain-Derived Neurotrophic Factor and Urokinase Plasminogen Activator Stimulates Peripheral Nerve Regeneration After Injury. J. Pharmacol. Exp. Ther. 2020;372(3):248−255
- Li L, Fang F, Feng X, Zhuang P, Huang H, Liu P, Liu L, Xu AZ, Qi LS, Cong L, Hu Y. Single-cell transcriptome analysis of regenerating RGCs reveals potent glaucoma neural repair genes. Neuron. 2022 Aug 17;110(16):2646-2663.e6. doi: 10.1016/j.neuron.2022.06.022. Epub 2022 Aug 10. PMID: 35952672; PMCID: PMC9391304



