Введение
В последние годы наблюдается значительный интерес к использованию биомассы морских водорослей в качестве возобновляемого источника энергии и сырья для производства фармацевтических препаратов. Данный тренд обусловлен не только экологической устойчивостью и экономической эффективностью такого подхода, но и перспективами в области биомедицины. В этом контексте представляется актуальным рассмотреть международный проект, реализуемый Акционерным Обществом Инвестиционная Холдинговая Компания «МИР», направленный на создание инновационных технологий для получения биотоплива, линейки аминокислот, противоопухолевых лекарственных средств и препаратов для лечения сахарного диабета 2 типа на основе водорослей.
Целью данного проекта является комплексное исследование биохимических и биотехнологических аспектов переработки морских водорослей, а также разработка и внедрение соответствующих производственных процессов. В рамках сотрудничества планируется использование научных достижений обеих стран для создания высокоэффективных и безопасных продуктов, способных внести значительный вклад в развитие мировой науки и промышленности.
Особое внимание в проекте уделяется изучению биоактивных компонентов водорослей, обладающих потенциалом в лечении онкологических заболеваний и сахарного диабета 2 типа. Речь идет о полисахаридах, полифенолах, каротиноидах и других биологически активных веществах, которые могут быть использованы в качестве основы для создания новых лекарственных препаратов.
С точки зрения энергетического аспекта, морские водоросли представляют собой перспективный источник биомассы для производства биотоплива. Их высокая продуктивность и способность к быстрому росту делают этот вид сырья привлекательным для разработки технологий получения биоэтанола, биогаза и других видов биотоплива.
Реализация данного проекта предполагает проведение комплексных исследований, направленных на изучение химического состава водорослей, разработку методов их культивирования и переработки, а также оптимизацию производственных процессов. Результаты этих исследований могут стать основой для создания новых технологий, способных значительно повысить эффективность использования морских водорослей в различных отраслях промышленности.
Таким образом, международный проект России и Кореи по производству биотоплива, аминокислот, противоопухолевых лекарств и препаратов от диабета 2 типа из водорослей представляет собой важное научное и технологическое достижение, способное внести значительный вклад в развитие мировой индустрии и науки.
Среди перспективных сырьевых ресурсов для получения биоэтанола выделяются морские водоросли, особенно бурые виды, такие как Saccharina japonica, широко распространённые в странах с развитой морской инфраструктурой, таких как Корея. Обоснованием актуальности данной идеи является высокая биомассовая продуктивность бурых водорослей, а также их богатство биохимическими компонентами, которые могут быть использованы для производства экологически чистого топлива. Данный проект нацелен на разработку и оптимизацию технологий получения биоэтанола из морской водоросли Saccharina japonica. Основная идея состоит в использовании биохимического потенциала водорослей для трансформации содержащихся в них сложных углеводов в спиртовой продукт через ферментационные процессы.
Это позволит значительно расширить сырьевую базу для производства биотоплива, повысить энергоэффективность технологических цепочек и снизить экологическую нагрузку на окружающую среду.
Задачи исследования включают изучение состава водоросли, оптимизацию условий предварительной обработки и ферментации, а также внедрение современных методов анализа и очистки конечного продукта. В качестве методов предполагается применение аналитических технологий, таких как газохроматография, для оценки выхода этанола и контроля качества продукции. Ожидается, что результаты работы позволят не только повысить выход биоэтанола из водорослей, но и обеспечить экологическую безопасность и масштабируемость технологий, что существенно для внедрения в промышленной сфере.
Значимость проекта заключается в возможности создания экологически безопасного и устойчивого источника энергии, который станет важным компонентом стратегии перехода к зелёной энергетике. Кроме того, данное исследование способствует развитию междисциплинарных направлений — биотехнологии, инженерии и экологии — и будет способствовать расширению практических знаний о переработке морской биомассы. В перспективе проект может содействовать укреплению энергетической независимости страны, развитию зеленой экономики и продвижению инновационных технологий в области производства биотоплива на мировой арене.
Актуальность выбранной темы обусловлена растущим спросом на экологически чистое и возобновляемое топливо, а также необходимостью поиска альтернативных источников энергии, особенно в условиях ограниченности традиционных ресурсов, таких как нефть и газ. Морские водоросли представляют собой богатый источник биоэнергетических веществ и обладают рядом преимуществ, включая быстрое возобновление, низкую требования к пресной воде и минимальное влияние на земельные ресурсы, что делает их перспективным сырьем для биотоплива, особенно в странах с развитой морской инфраструктурой, таких как Корея.
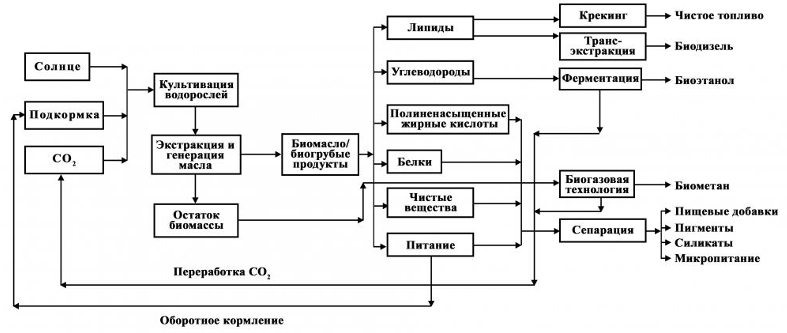
Ожидаемые результаты включают разработку технологического протокола, позволяющего повысить выход биоэтанола из морской водоросли, улучшение его качества и экологической безопасности, а также показатели эффективности процесса. Перспективы исследования связаны с возможностью масштабирования технологической схемы и внедрения в промышленное производство, что позволит снизить зависимость от ископаемых видов топлива, уменьшить экологический след энергетической отрасли и стимулировать развитие биотехнологической сферы в регионе. Для достижения поставленных целей будут использованы комбинации методов химической и биологической обработки, аналитической диагностики и технологического моделирования, что обеспечит комплексный подход и практическую применимость результатов.
В современном мире проблема поиска экологически чистых и устойчивых источников энергии становится все более актуальной в связи с истощением традиционных ископаемых ресурсов и негативным воздействием их эксплуатации на окружающую среду. В контексте этой ситуации особое значение приобретает разработка альтернативных видов топлива, одним из наиболее перспективных из которых является биоэтанол, полученный из возобновляемых сырьевых источников. Морские водоросли, в частности бурые водоросли, обладают значительным биохимическим потенциалом для производства биоэтанола благодаря высокой биомассе и богатому содержанию полисахаридов, пригодных для ферментации. Тем не менее, на сегодняшний день используемые подходы к синтезу этанола из водорослей сталкиваются с рядом технологических и экологических проблем, таких как низкая эффективность методов предварительной обработки сырья, ограниченная оптимизация условий ферментации, сложности в сепарации конечного продукта и недостаточная масштабируемость существующих процессов. Кроме того, многие из современных технологий требуют значительных энергетических затрат и имеют потенциальные экологические риски при интенсивной эксплуатации водорослей в природных экосистемах, что требует поиска более экологичных и устойчивых решений. Анализ существующих подходов показывает, что несмотря на активные исследования в данной области, практически не достигнута существенная степень их коммерциализации и внедрения в промышленность. Одной из причин является отсутствие универсальных технологий, позволяющих эффективно и экологично превращать морскую биомассу в биоэтанол при минимальных затратах. Также недостаточно изучены особенности биохимического состава различных видов морских водорослей, что тормозит разработку оптимальных методов ферментации и обработки сырья.
Задачи
Основной целью данной исследовательской работы является разработка эффективных методов получения биоэтанола из морских водорослей, с особым акцентом на бурые водоросли, такие как Saccharina japonica, которые широко распространены и обладают высоким потенциалом для производства возобновляемого топлива.
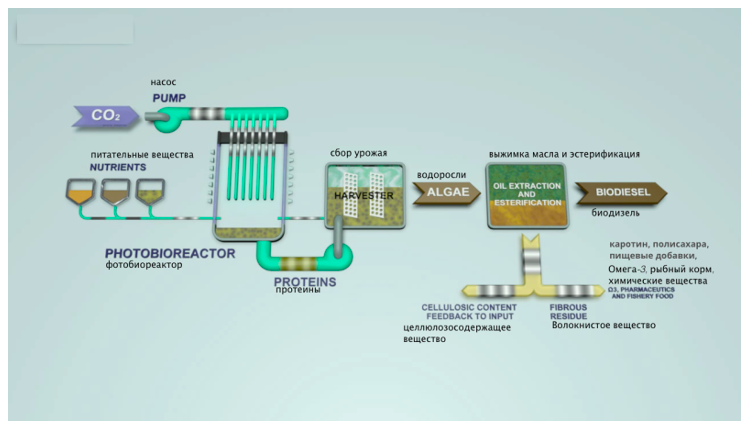
Для достижения этой цели сформулированы несколько комплексных задач, направленных на углубленное исследование биохимического состава водорослей, оптимизацию технологических процессов и повышение выхода конечной продукции при сохранении экологической безопасности.
Первая задача заключается в анализе биохимического состава морских водорослей, выявлении ключевых компонентов, пригодных для последующей ферментации и синтеза этанола. Этот этап включает проведение лабораторных анализов с использованием современных методов химического и микробиологического исследования, что позволит определить оптимальные исходные сырьевые материалы и параметры подготовки водорослей к переработке.
Следующая задача — разработка и оптимизация процесса экстракции и подготовки биомассы для ферментации. Это предполагает исследование различных методов механической и химической обработки, а также определение условий, способствующих максимальной биодоступности и эффективности ферментационных процессов.
Особое внимание уделяется оптимизации условий ферментации, включая выбор микроорганизмов, температуры, pH и других технологических параметров. В рамках этой задачи планируется протестировать различные штаммы дрожжей и бактерий, а также разработать технологии повышения эффективности ферментационных процессов для получения наиболее чистого и высокого выхода этанола.
Дополнительной задачей является проведение дистилляционных процедур для разделения и очистки биоэтанола, а также внедрение современных методов аналитики, таких как газохроматография, для точной оценки состава и выхода продукта. Это позволит обеспечить качество продукции и подтвердить эффективность разработанных технологий.
Кроме того, важной задачей является оценка экономической и экологической эффективности предложенных методов, анализ затрат и возможных рисков, а также разработка рекомендаций по внедрению технологий в промышленные масштабы. В ходе исследования предполагается разработать комплексный план, объединяющий лабораторные и пилотные этапы, что обеспечит возможность масштабирования результатов и их практического применения.
Все обозначенные задачи служат основой для последовательного достижения научных и практических целей проекта, расширения знаний о возможностях использования морских водорослей в биоэнергетике, а также для формирования научных рекомендаций по развитию экологически чистых источников топлива в контексте современных вызовов энергетики и охраны окружающей среды.
Теоретическая основа исследования
Биохимия морских водорослей и их потенциал для производства биоэтанола
Биохимия бурых водорослей характеризуется сочетанием уникальных полисахаридов, углеводных запасов и мелких вторичных веществ, что определяет их потенциал как сырья для биоэтанола. Важнейшими компонентами являются ламинарин — запасной полисахарид, состоящий преимущественно из β-1,3-глюкана с вторичными связями β-1,6; маннитол — водорастворимый сахаро-алкоголь, накапливающийся в клетках как основное углеродное хранилище; и структурные/функциональные полисахариды, такие как альгинат и фукоидан, а также целлюлоза, входящая в клеточную стенку. Такой состав определяет как потенциальность образования этанола, так и требования к предобработке и ферментации — разложению сложных углеводов на ферментируемые сахара.
Выделение ключевых компонентов для производства биоэтанола требует системного анализа их биохимических свойств и биотехнологических возможностей трансформации. Ламинарин обеспечивает обогащение глюкозой после гидролиза, но его частичный распад требует специфических ферментов (ламинариназы, β-глюканозы) и адаптированных условий экстракции.
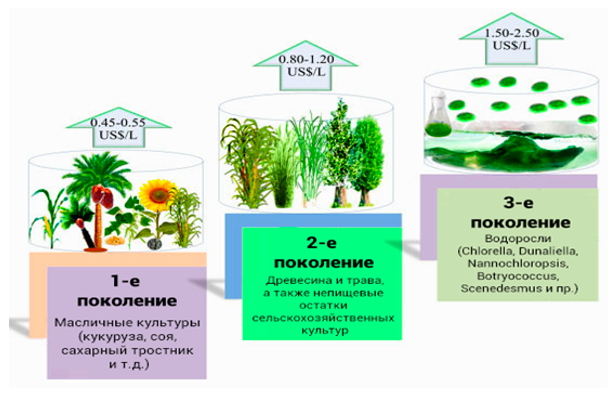
Методы экстракции и переработки полисахаридов бурых водорослей включают физическую сушку и измельчение, водное экстрагирование и применение ферментов для гидролиза. Горячее водяное или щелочно-кислотное экстрагирование позволяет сосредоточить ламинарин и маннитол, после чего следует селективная гидролиз laminarin до глюкозы с использованием ламинариназ и смежных ферментов (β-глюканозы, глюканомонооксидазы). Современные подходы предусматривают сочетание физико-химической предобработки и enzymatic hydrolysis для повышения выхода ферментируемых сахаров, а затем последующую ферментацию. Экологическая безопасность технологий требует выбора биореакторов и условий, минимизирующих образование токсичных побочных продуктов и снижений активности ферментов, а также эффективного контроля содержания растворённых солей и альгинатов, которые могут ингибировать микроорганизмы.
Перспективы масштабирования в энергетической сфере зависят от эффективности конверсии основных компонентов в этанол и сочетания с устойчивыми цепочками получения вторичных полезных продуктов. Для бурых водорослей характерно отсутствие потребности в пахотной земле и возможность представительской биокультивации в морских системах, что особенно актуально для Кореи и регионов с развитыми аквакультурными инфраструктурами.
Методы обработки морской водоросли для ферментации
Методы обработки бурых водорослей для ферментации направлены на эффективное высвобождение ферментируемых сахаров при минимальном образовании ингибиторов и с учетом особенностей биохимического состава бурых водорослей. Введение предварительной обработки должно обеспечить доступ к основным сахарам ламинарина, маннитолу и другим полисахаридам, сохранив при этом энергетическую и экологическую эффективность технологии.

Процесс начинается с сбора и сортировки бурых водорослей (например Saccharina japonica) с целью удаления посторонних материалов и солевых примесей. Далее следует очистка и промывка для снижения концентрации солей и минералов, что важно для снижения осмотического стресса у микроорганизмов-производителей этанола. После этого водоросли подвергают сушки или фриз-заморозке для стабилизации массы и уменьшения влаги до уровня, удобного для измельчения. Мелкие фракции обеспечивают более однородную обработку полисахаридов и улучшают проникновение ферментов. Параллельно проводится контроль влажности, содержания солей и общего углеводного потенциала, что критично для планирования последующих стадий гидролиза. Важна также минимизация образования ингибиторов после гидролиза за счет оптимальной температуры и времени обработки.
Выбор микроорганизмов должен учитывать наличие в субстрате глауцозы от ламинарина и маннитола, а также соленость исходного сырья. Для большинства этанол-производящих систем применяют дрожжи класса Saccharomycetes (рекомендуются штаммы Saccharomyces cerevisiae) благодаря высокой этаноловой урожайности и устойчивости к умеренной солености. Однако бурые водоросли богаты маннитолом и сложными углеводами, для обработки которых привлекают альтернативные или инженерно-модифицированные штаммы: Kluyveromyces marxianus, некоторые виды Pichia и Candida, а также устойчивые к солености штаммы Saccharomyces spp. Возможно применение консорциумов микроорганизмов, где одни микроорганизмы специализируются на гидролизе полисахаридов, а другие — на ферментации глюкозы и маннитола. Перспективны также штаммы с улучшенной толерантностью к соли и высоким темпам роста в гиперосмолярной среде. В перспективе эффективна интеграция генетически модифицированных штаммов, способных к ферментации более широкой совокупности сахаров, а также к переработке промежуточных продуктов гидролиза.

Оптимальные параметры зависят от выбранного штамма и стадии процесса. Рекомендованы следующие ориентиры: температура ферментации 28–34 °C, pH 4,5–5,5 для большинства дрожжей; продолжительная анаэробная фаза после адаптивной аэробной стадии, с подачей субстрата по ступеням или в виде fed-batch для поддержания концентрации сахаров и уменьшения котаболитов. Солёность рабочей среды должна соответствовать условиям роста водорослеалергических штаммов и не препятствовать ферментации; типично поддерживать умеренную соленость, совместимую с выбранной стратегией микроорганизмов. Рекомендуется применение предварительных стадий адаптации клеток к солёной среде и субстратному стеклу, чтобы повысить выход этанола и снизить образование побочных продуктов. Внедрение стратегий биореакторной инженерии, таких как SSF или fed-batch режимы, позволяет снизить инверсию сахаров и повысить общую эффективность процесса. Особое внимание уделяют контролю ингибиторов, температуры и времени гидролиза, чтобы снизить энергозатраты и повысить устойчивость технологического цикла.
Ключевые показатели анализа сосредоточены на выходе этанола, составе смесей и потенциале повторного использования остаточных субстратов. Этанол квалифицируют по объему и массе, проводят количественный анализ сахаров до и после ферментации, используя HPLC или аналогичные методы. Газохроматографический анализ целевых и побочных спиртов (GC-FID/GC-MS) обеспечивает точную оценку чистоты этанола и примесей. Дополнительно применяется спектроскопия и тензометрический анализ для оценки концентраций растворённых веществ и потенциальных ингибиторов. Важны экологические аспекты: оценка выбросов энергии, образования токсичных побочных продуктов и возможности повторного использования биомассы как части биотопливной цепи.

Расширение применения консорциумов микроорганизмов и инженерных штаммов позволяет увеличить спектр конвертируемых углеводов бурых водорослей в этанол. Интеграция ферментации с гидролизом в рамках единого биореактора (SSF) снижает потребность в дополнительных стадиях и снижает энергозатраты. Развитие устойчивых к солёности штаммов и адаптация процессов к промышленным условиям открывают путь к масштабированию. В перспективе данные технологии могут быть внедрены в биотопливно-энергетические кластеры Кореии и регионов с доступом к бурым водорослям, способствуя более устойчивым подходам к производству биоэтанола и созданию замкнутых биотехнологических циклов.
Процессы ферментации, дистилляции и анализ состава спиртов
В данной подсекции рассматриваются ключевые этапы получения биоэтанола из бурых водорослей с акцентом на процессы ферментации, дистилляции и последующего анализа состава получаемых спиртов. Исходной сырьевой базой являются бурые водоросли (например, Saccharina japonica), богатые глюканами laminaran и маннитолом, требующие предварительной обработки для высвобождения ферментируемых углеводов. Ферментацию осуществляют микробные сообщества и штаммы, способные перерабатывать глюкозу и вторичные сахара водорослей, обеспечивая устойчивость процесса к морской солевой среде и специфическим микробиоингредиентам.
Условия ферментации характеризуются умеренно кислой средой и умеренной температурой: pH примерно 4,5–5,5, температура 25–35 °C, без кислородной агитации или с минимальным уровнем газа. Важна предварительная очистка и минимизация ингибиторов, которым служат солевые остатки и продукты распада, возникающие при гидролизе. В зависимости от состава водорослей и режима гидролиза возможно использование однокомпонентной или ко‑ферментации, когда альтернативно выделяются углеводы, позволяющие обеспечить более высокий выход этанола. Оценка эффективности основывается на выходе этанола на единицу массы исходного субстрата и на массо-энергетическом балансе процесса..
Аналитика состава спиртов опирается на традиционные и современные методы химического анализа. В качестве основного метода количественной оценки этанола применяется газовая хроматография с детектором пламенного ионизационного детекции (GC‑FID). Образцы подготавливают путём разбавления и, по необходимости, headspace‑анализа, применяя внутренний стандарт для точности измерений. Современные методики предусматривают оценку не только содержания этанола, но и сопутствующих компонентов и примесей: ацетальдегида, метанола,Higher alcohols (фузельные масла) и органических кислот. Для контроля углеводной фракции применяют ВЧ‑ХПЛХ (HPLC) с детектором РИД для анализа сахаров и олигосахаридов, а также спектрометрический анализ (GC‑MS) для идентификации летучих соединений и побочных продуктов. Совокупность методов позволяет формировать портфель показателей качества: выход этанола, чистота продукта, содержание воды и примесей, соответствие нормативам биотоплива. Важным элементом является метрический подход к верификации методик: калибровка, валидация, повторяемость и воспроизводимость результатов.
Эталонные принципы обеспечения качества и безопасности продукции включают мониторинг процесса на всех стадиях: от гидролиза до финального обезвоживания. В частности, влияние флоты и коэффиценты растворимости, а также содержание посторонних и токсичных соединений должны контролироваться на каждой ступени. Комплексный подход к анализу способствует минимизации рисков, повышению устойчивости к вариациям состава водорослей и обеспечению совместимости с требованиями стандартов биотоплива.
Практическая часть
Подготовка образцов Saccharina japonica
Подготовка образцов Saccharina japonica является ключевым этапом практической части проекта по получению биоэтанола. Формирование единых требований к сбору, очистке, сортировке и хранению обеспечивает воспроизводимость экспериментов и сопоставимость результатов между лабораторными сериями.

Важно учитывать сезонность, биологическое состояние растений и условия окружающей среды. Как отмечено в источнике, «весенне-осенние данные по гидрохимическим показателям и структуре фитопланктона» являются критерием отбора образцов для дальнейших процедур. Данные принципы применяются при выборе участков сбора и периодов выполнения работ, что позволяет минимизировать вариации, связанные с внешними факторами.
Методы сбора образцов
Методы сбора рассчитываются так, чтобы минимизировать повреждения тканей и обеспечить репрезентативность образцов. В полевых условиях применяются ручной сбор и срезка длинных фрагментов у молодого и зрелого организма на глубинах, соответствующих культивированному и естественному состоянию растений. Этапы включают: выбор участков с однородной характеристикой средовых условий, фиксацию времени сбора и фиксацию разместившихся на берегу элементов. Важна совместимость сырья по размеру фрагментов, что обеспечивает сопоставимость последующих этапов гидролиза и ферментации. После сбора образцы размещают в прочных сетчатых мешках или специальных контейнерах, обеспечивающих вентиляцию и защиту от механических повреждений, с минимальным временем от сбора до очистки. Такой подход снижает риск акклиматизации тканей и потери углеводных резервов.
Очистка и сортировка
Очистка проводится для удаления посторонних материалов (эпифитов, песка, частиц донных осадков) и возможной биоты, которая может влиять на результаты анализа. Рекомендуется промывание образцов в морской воде или фильтрованной морской воде с последующим аккуратным встряхиванием и просушиванием на сетках с минимальным контактом с воздухом. Сортировка предполагает разделение по размерам и целостности ткани: исключаются участки с четкими разрывами, гнилью или признаками патогенеза. Применение единообразных критериев отбора обеспечивает сопоставимость данных между партиями образцов. Проводимый визуальный осмотр сопровождается фиксированием массы и длины фрагментов на каждом этапе подготовки.
Хранение и контроль качества образцов
После очистки образцы приводят к стандартной форме хранения: фиксация идентификационных меток, учетная запись даты и места сбора, условия транспортировки и времени до начала обработки. Для краткосрочного хранения применяют холодовую цепь: охлаждение до 0–4 °C с минимальным временем между доставкой в лабораторию; для долгосрочного хранения допускается заморозка при −20 °C или ниже, либо высушивание до стабильного сухого веса в условиях контролируемой влажности. Этап подготовки к экспериментам включает документирование всех параметров: источник сбора, глубину, сезон, метод очистки, размер фрагментов, влажность и масса, условия хранения. Такая информация критична для корректного нормирования процессных данных, сопоставления показателей выхода этанола и анализа эффективности в рамках следующего подраздела 3.2 и для обеспечения прозрачности методики.
Ферментация и дистилляция биоэтанола
В разделе рассматриваются основные стадии процесса: ферментация и дистилляция биоэтанола из бурых водорослей Saccharina japonica, а также параметры, оборудование и методы их оптимизации. Особое внимание уделяется повышению выхода этанола, качеству продукта и снижению энергетической потребности циклических процессов, что повышает экологическую безопасность технологии в условиях морской биотехнологии.
Этап ферментации выполняется с использованием штаммов дрожжей, устойчивых к солоноватой среде и способных перерабатывать сахара, полученные из ламинарина и сопутствующих полисахаров. Оптимальные условия ферментации включают pH 4,5–5,5, температуру 28–32 °C, аэробный старт с последующим переходом к анаэробному режиму, а также нутриентное обогащение азотом и микроэлементами. Важной задачей является выбор стратегии конверсии маннитола и других редуцированных сахаров в этанол без существенного образования побочных продуктов, что требует интеграции специализированных штаммов и/или стадий ферментации (гибридные или двухступенчатые схемы).
Дистилляция представляет собой этап разделения этанола и водной фазы с целью достижения требуемой твердой фазы этанола. Рассматриваются как пакетные, так и непрерывные схемы дистилляции, возможность использования вакуумной дистилляции для снижения энергозатрат и ограничения образования перегретой воды. Важным аспектом является дегидратация этила до конкретной чистоты: для биотопливного применения целевой показатель достигается с применением сиропа молекулярного ситового удаления или вакуумной фракционной дистилляции, что позволяет получить этанол 99,5% без значительных примесей. Энергопотребление дистилляции оценивается через коэффициент теплообменника и эффективность регенерации тепла на стадии рекуперации энергии, что особенно критично при работе с морскими водорослями, где требуется адаптация к соленой воде и устойчивым условиям.
Оценка эффективности процесса проводится по нескольким показателям: выход этанола на единицу массы исходной биомассы, коэффициент конверсии сахаров в этанол, энергия на единицу полученного этанола и уровень образования побочных продуктов. Современные подходы предполагают использование интегрированных схем теплообмена, совместной подготовки и переработки побочных фракций, а также анализ экономичности за счет снижения капитальных затрат на установку и операционных затрат на энергию. Важной целью является снижение общего энергетического следа цикла ферментации-дистилляции за счет оптимизации режимов ферментации, точной регулировки условий дистилляции и эффективной дегидратации.
Газохроматографический анализ и оценка выхода этанола
Газохроматографический анализ представляет собой ключевой компонент оценки выхода этанола на этапе практической части проекта. Для определения концентрации этанола в буровом среде применяются методы газовой хроматографии с фотовидовым детектированием (FID) или масс-спектрометрическим детектированием (GC-MS). Выбор метода определяется требуемой чувствительностью, селективностью к этанолу и степенью matrix-пригодности образца. На практике предпочтение может быть отдано газохроматографии с инжекцией в голодной или головочной паре (headspace, HS-GC), поскольку она минимизирует влияние солей и растворителей, характерных для ферментационных сред бурых водорослей, и сокращает подготовку образца.
Условия газохроматографа подбираются так, чтобы обеспечить четкую разделимость этанола от сопутствующих летучих соединений, минимизировать смещение времени reten-tion и обеспечить воспроизводимость. Типичная колонка с полярной или полярно-неполярной фазой длиной около 30 м и внутренним диаметром 0,25–0,32 мм, совместимая с водой и органическими растворителями, может использоваться вместе с газовым захватом He или N2 как переносчиком. Температурный режим включает стартовую температуру около 40–60°C с медленным нарастанием до 120–150°C, что обеспечивает плавную элюиацию этанола и минимизирует перекрытие с водой. Инжектор обычно устанавливают на 200–250°C, детектор FID — на 250–300°C. В случае GC-MS регистрируются их масс-спектры для дополнительного подтверждения массы молекулы этанола и параметров примесей.
Калибровка осуществляется на матричном образце, близком к породе измеряемой пробы. Стандартная калибровочная серия включает несколько концентраций этанола в водной или матричной среде, с добавлением внутреннего стандарта. Построение линейной зависимости площади пика этанола к концентрации обеспечивает линейность выше R2 = 0,99 в диапазоне содержания, соответствующем ожидаемым величинам в процессе ферментации. Предел обнаружения (LOD) и предел количественного определения (LOQ) оцениваются по стандартной методике через сигма-корреляцию динамики базового уровня и величину превышения относительно шума.
Применение данного подхода обеспечивает надёжную идентификацию этанола и позволяет объективно оценивать эффективность процесса ферментации и качество продукции. Значимые различия между экспериментальными сериями свидетельствуют о влиянии операционных параметров и состава исходной биомассы на выход продукта. В рамках проекта данные GC-анализа служат основой для оптимизации условий ферментации, снижения затрат энергии и повышения экологической безопасности технологий. «Газохроматография обеспечивает точное и воспроизводимое определение этанола в сложных биологических матрицах».
Общие выводы по результатам проведенного исследования свидетельствуют о высокой потенциальной ценности морских водорослей, в частности бурых водорослей типа Saccharina japonica, в качестве сырья для производства биотоплива, в частности биоэтанола.
Полученные данные продемонстрировали, что использование морских водорослей позволяет не только обеспечить стабильное сырьевое обеспечение, но и значительно снизить экологическую нагрузку по сравнению с традиционными источниками энергетики. Биохимический состав водорослей, богатство полисахаридами и присутствие ферментируемых веществ создают прочную основу для разработки эффективных технологических решений по их обработке, ферментации и последующей очистке биоэтанола.
Источники финансирования
Эмиссия АО ИХК «МИР» составляет 150 миллионов акций по цене определенной ЦБ РФ в 1 тысяча рублей за одну ценную бумагу.
В целях мобилизации необходимых финансовых ресурсов планируется осуществить дополнительную эмиссию ценных бумаг в неограниченном объеме, что соответствует требованиям Федерального закона № 39-ФЗ "О рынке ценных бумаг" от 22 апреля 1996 года.
Аминокислоты
В бурых водорослях идентифицировано 23 свободные аминокислоты, представляющие собой ключевые компоненты их биохимического состава. Среди них выделяются такие важные аминокислоты, как аланин, аллоизолейцин, аргинин, аспарагиновая кислота, хондрин, цистеиновая кислота, D-цистеиноливая кислота, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, орнитин, фенилаланин, пролин, серин, таурин, треонин, триптофан, тирозин и валин. Эти данные подтверждены исследованиями, опубликованными на платформе CyberLeninka.
Наиболее высококонцентрированными аминокислотами в бурых водорослях являются аланин, глутаминовая кислота, глицин, пролин и треонин. Среди незаменимых аминокислот особое место занимает лизин, который также встречается в значительных количествах. Эти данные были опубликованы в авторитетных научных источниках.
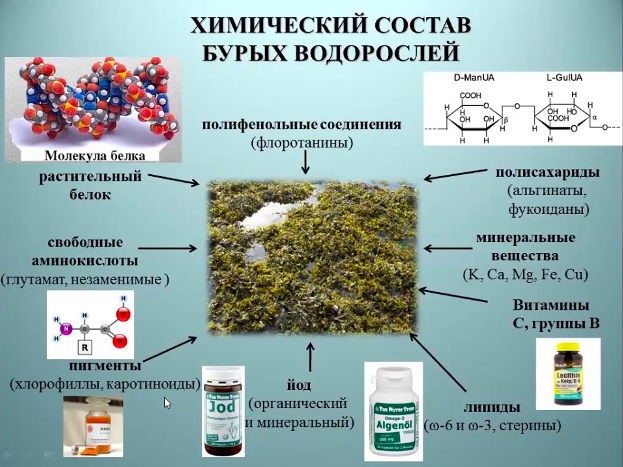
Уникальной особенностью аминокислотного состава бурых водорослей является присутствие йодоаминокислот, таких как моно- и дийодтирозин, что подчеркивает их специфическую биохимическую природу и потенциальные функциональные свойства.
Состав и концентрация свободных аминокислот в бурых водорослях значительно варьируются в зависимости от видовой принадлежности, условий произрастания и времени сбора. Например:
- Водоросли, произрастающие на Камчатском побережье, содержат 15–20 индивидуальных аминокислот, среди которых аспарагиновая кислота, глутаминовая кислота и аланин являются наиболее распространенными.
- Фукусовые водоросли Белого моря характеризуются наличием 18 аминокислот, из которых 7 являются незаменимыми.
- У водорослей вида F. vesiculosus, независимо от места произрастания, доминируют аспарагиновая и глутаминовая кислоты. Однако, F. vesiculosus, собранные в Белом море, отличаются повышенным содержанием гистидина, в то время как в Балтийском и Баренцевом морях в составе свободных аминокислот преобладают аланин и пролин.
Эти данные свидетельствуют о высокой степени адаптивности бурых водорослей к различным экологическим условиям и подчеркивают важность дальнейших исследований в этой области для понимания их биохимического потенциала и возможностей применения.
ПРОТИВООПУХОЛЕВАЯ И АНТИМЕТАСТАТИЧЕСКАЯ АКТИВНОСТЬ СУЛЬФАТИРОВАННОГО ПОЛИСАХАРИДА ФУКОИДАНА БУРОЙ ВОДОРОСЛИ
Фукоиданы представляют собой класс полианион‑ ных разветвленных гомо‑ и гетерополисахаридов, состоящих преимущественно из остатков сульфатиро‑ ванной α‑L‑фукозы. Основным источником фукоиданов являются все виды бурых водорослей, однако в наибольших концентрациях они присутствуют в двух видах – Fucales и Laminares. Кроме бурых водорослей фукоиданы встречаются также в тканях некоторых морских беспозвоночных.
Впервые сульфатированный полисахарид «фукоидан» из морских бурых водорослей был выделен еще в 1913 г., и длительное время он рассматривался главным образом в качестве источника L‑фукозы. В настоящее время интерес к этому классу полиса‑ харидов значительно возрос в связи с полученными в последние десятилетия сведениями о их биологической активности: антикоагулянтной, антитромбической, противовоспалительной, антивирусной, иммуностимулирующей и противоопухолевой, что связывают со способностью этих полисахаридов взаимодействовать с рядом белков и влиять на свойства клеточной поверхности .
Противоопухолевая и антиметастатическая активность фукоиданов из различных источников была продемонстрирована на моделях мышиных опухолей in vivo и в экспериментах in vitro. Было показано, что фукоиданы участвуют в таких клеточных процессах, как миграция, адгезия, рост и апоптоз клеток, играющих важную роль в механизмах неотрансформации против опухолей.
Морские водоросли Корейского побережья и сахарный диабет 2 типа
Съедобные бурые водоросли нормализуют уровень глюкозы у пациентов с диабетом второго типа и поможет в профилактике этого заболевания у здоровых людей. Исследование показало, что у пациентов, употреблявших морские водоросли, показатели глюкозы в крови постепенно стабилизировались.
Сахарный диабет второго типа составляет 98% всех случаев заболевания, нарушающего способность организма перерабатывать сахар. Болезнь опасна тем, что ей сопутствуют рак, сердечно-сосудистые нарушения и другие состояния, угрожающие жизни пациента.
От диабета невозможно избавиться навсегда, и человек вынужден постоянно контролировать уровень глюкозы в крови с помощью медикаментов. Бурые морские водоросли могут стать естественной альтернативой некоторым лекарствам, не имея при этом побочных эффектов.
Список литературы
- С.З, Алиева, Р.А. Ахмедханова. Морские водоросли и крапива для бройлеров // Животноводство России. 2025. URL: https://zzr.ru/zzr-2025-04-003 (дата обращения: 11.02.2026). DOI: 10.25701/zzr.2025.04.001
- И.И. Кочиш. МОРСКИЕ ВОДОРОСЛИ: ПОТЕНЦИАЛ ИСПОЛЬЗОВАНИЯ В РАЦИОНАХ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ (обзор) // Sel'skokhozyaistvennaya Biologiya. 2023. URL: http://www.agrobiology.ru/6-2023kochish.html (дата обращения: 11.02.2026). DOI: 10.15389/agrobiology.2023.6.1006rus
- С. В. Емец. «Морские черепахи» и «водоросли»: нарративизация возвращения на родину китайских выпускников сибирских университетов // Tomsk Journal of Linguistics and Anthropology. 2025. URL: https://ling.tspu.ru/archive.html?year=2025&issue=2&article_id=9448 (дата обращения: 11.02.2026). DOI: 10.23951/2307-6119-2025-2-131-142
- Л. И. Рябушко, А. Г. Широян, Д. Н. Лишаев. Диатомовые водоросли эпифитона макрофитов крымского прибрежья Чёрного моря // Труды Карадагской научной станции им. Т.И. Вяземского - природного заповедника РАН. 2021. URL: https://eco-ibss.ru/jour/article/view/112 (дата обращения: 11.02.2026). DOI: 10.21072/eco.2021.15.01
- И. К. Евстигнеева, И. Н. Танковская. БИОМАССА МАКРОФИТОБЕНТОСА И ЕЕ РАСПРЕДЕЛЕНИЕ ВДОЛЬ ЗАПАДНОГО БЕРЕГА КРЫМСКОГО ПОЛУОСТРОВА (ЧЕРНОЕ МОРЕ) // Российский журнал прикладной экологии. 2023
- Т.В. Пилипенко, Д.Ю. Куприянов, М.А. Ширяева, В В Турбинский. Биоэкологические исследования озера Манжерокское // Гидросфера. Опасные процессы и явления. 2025
- М.В. Макаров, Л.В. Бондаренко, В.Г. Копий. Донная фауна бухты Круглой (Чёрное море, Крым). Сообщение 1. Эпифитон макрофитов // Труды Карадагской научной станции им. Т.И. Вяземского - природного заповедника РАН. 2022. URL: https://eco-ibss.ru/jour/article/view/162 (дата обращения: 11.02.2026). DOI: 10.21072/eco.2022.21.02
- Молдрахман А.С., Мажибаева Ж.О., Долгополова С.Ю, Кожижанова Б.А, Cүлейменова А.М. ГИДРОХИМИЧЕСКИЕ ИССЛЕДОВАНИЯ И ФИТОПЛАНКТОН СОЛЕНЫХ ОЗЁР ПАВЛОДАРСКОЙ ОБЛАСТИ // HERALD OF SCIENCE OF S. SEIFULLIN KAZAKH AGRO... 2022
- Журавлев Р.А., Дунец Е.Г., Джум Т.А., Тамова М.Ю. ТЕХНОЛОГИЯ ПРОИЗВОДСТВА И КОНТРОЛЬ КАЧЕСТВА БИСКВИТА С ВКЛЮЧЕНИЕМ ПОРОШКА ИЗ ВОДОРОСЛЕЙ // Ползуновский вестник. 2023
- М. И. Мустафаева. ФЛОРИСТИЧЕСКИЙ СОСТАВА ВОДОРОСЛЕЙ И О ЗАКОНОМЕРНОСТЯХ ИХ РАЗВИТИЯ // Advances in Science and Environment. 2025
- С. Б. Нурашов, Э. С. Саметова, А. К. Джиенбеков. Таксономический состав водорослей реки Шолаканкаты Сырымского района Западно-Казахстанской области // Spiraeanthus. 2025
- Я. Ю. Григорьев, А. Л. Григорьева, И. Н. Альхименко. Оценка динамики распространения водорослей в прибрежных зонах при помощи компьютерного зрения // MORSKIE INTELLEKTUAL`NYE TEHNOLOGII. 2025
- М. П. Клиндух, И. В. Рыжик, М. Ю. Меньшакова. СЕЗОННЫЕ ОСОБЕННОСТИ СОДЕРЖАНИЯ СВОБОДНЫХ АМИНОКИСЛОТ В РАЗНЫХ УЧАСТКАХ ТАЛЛОМА БУРОЙ ВОДОРОСЛИ FUCUS VESICULOSUS L. БАРЕНЦЕВА МОРЯ, "Наука юга России" // Science in the South of Russia. 2023
- С. Л. Полякова, С. Н. Железнова, Р. Г. Геворгиз, Н. А. Давидович. Эколого-физиологические характеристики и биотехнологический потенциал диатомовой водоросли Nitzschia amabilis H. Suzuki // Физиология растений. 2023
- У. А. Васильева. ВЗАИМОСВЯЗЬ МЕТАБОЛИЗМА ЖИРНЫХ КИСЛОТ И ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ У ДВУХ ВИДОВ БАЙКАЛЬСКОЙ ЭНДЕМИЧНОЙ ВОДОРОСЛИ DRAPARNALDIOIDES // Вестник Бурятского государственного университета. Биология, география. 2023



